单B细胞抗体技术的关键步骤
单个B细胞抗体技术作为新一代抗体开发技术,可以从单个B细胞中高效、快速的分离抗体,是继杂交瘤、噬菌体展示后又一抗体产生技术的突破。它是根据每一个B细胞只含有一个功能性重链可变区DNA序列和一个轻链可变区DNA序列,以及每一个B细胞只产生一种特异性抗体的特性,从免疫动物组织或外周血中分离抗原特异性B细胞,通过单细胞PCR技术从单个抗体分泌B细胞中扩增IgG重链和轻链可变区基因,然后在哺乳动物细胞内表达获得具有生物活性的单克隆抗体。
这种技术的特点,是“从打过胜仗的老兵身上找武器”。一是省去了先用抗原免疫小鼠这一步,二是不再依赖必须与骨 髓瘤杂交的小鼠B细胞。有了这一段基因,无论插到什么细胞都可以培养并量产,其效果类似大肠杆菌生产基因重组人胰岛素。

典型的单个B细胞技术流程
它的主要流程为先从免疫动物或人的身上获取外周血单个核细胞,再进行抗原特异性结合B细胞的分选,接着通过PCR扩增技术得到单个B细胞抗体可变区基因,再通过载体构建获得抗体表达,最 后进行产物验证。在此过程中,单个B细胞的分离是单B细胞技术最关键的步骤。目前有多种基于单细胞分离的技术,如磁珠分选法、微雕刻和ISAAC方法,流式分选法及微流控分选法等。
流式分选法是目前单B细胞技术应用较广泛的一种,它是基于抗原抗体的特异性反应,利用荧光素标记的B细胞表面分子的抗体以及标记的特异性抗原,通过多色流式分析与分选,筛选抗原特异性B细胞。流式分选可以直接将单个抗原特异性B细胞分选入细胞培养板的单孔中,进行后续的抗体基因扩增与测定。该技术优点:分离B细胞快速、准确、大量、多参数同时分析。
丹纳赫生命科学旗下贝克曼库尔特的CytoFLEX SRT分选型流式细胞仪是新一代的高效细胞分选平台,适用于多色免疫分型,可进行稳定高表达细胞系的开发、单细胞测序应用等。CytoFLEX SRT流式细胞分选仪提供七种不同检测器配置,多达 15 种荧光颜色用于区分细胞群,能够区分细胞间的细微差异,多色应用超高灵敏度提高筛选精度;拥有4 路分选模式、混合分选模式、复杂分选逻辑等分选方式,能够捕捉其他分选液流中丢弃的细胞,并保存宝贵细胞。

贝克曼库尔特CytoFLEX SRT流式细胞分选仪
CytoFLEX SRT流式细胞分选仪使用垂直分选模式(Straight Down Mode),利用无电垂直向下的液流,而不是加载电荷的偏转液流。在进行单细胞索引分选时,使用这种模式可以在精确分选单细胞的同时获得更好地分选后活率。
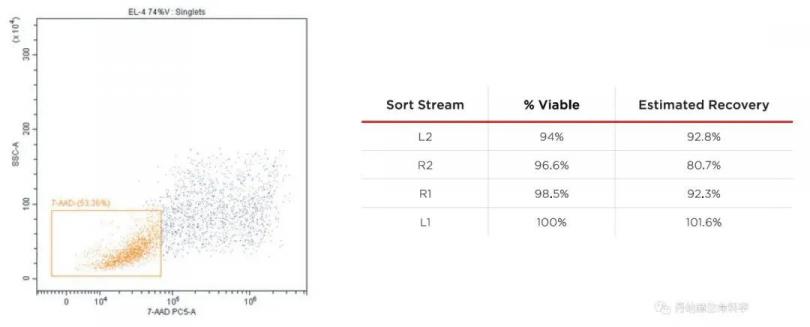
贝克曼库尔特VICELL-XR评估
EL4小鼠T细胞淋巴瘤细胞的培养后活率
CytoFLEX SRT配套的数据获取和分析软件界面直观,方便多色分析;采用创新的设置、监测和液流维持系统,实现工作流自动化,节省研发者大量时间和精力。
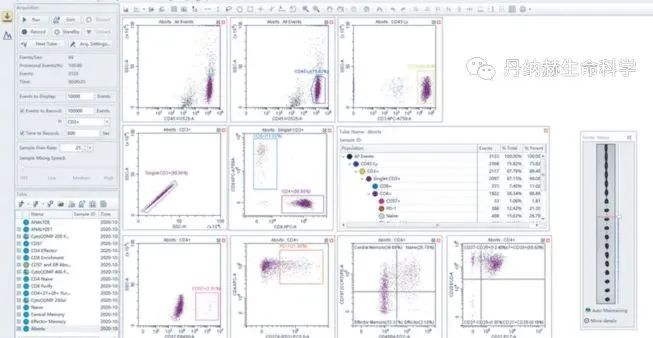
CytEXPERT SRT软件界面
此外,美谷分子仪器的CloneSelect 高通量单细胞分离系统,基于微流控分离技术,使用专有的喷墨式一次性单向分离槽,可以轻柔而高效地分离单个细胞。该系统拥有高分辨率的明场和荧光成像,可以对细胞进行分选图像采集,获得单克隆的图像证据,具有潜在的单个B细胞分离的应用价值。

CloneSelect 高通量单细胞分离系统
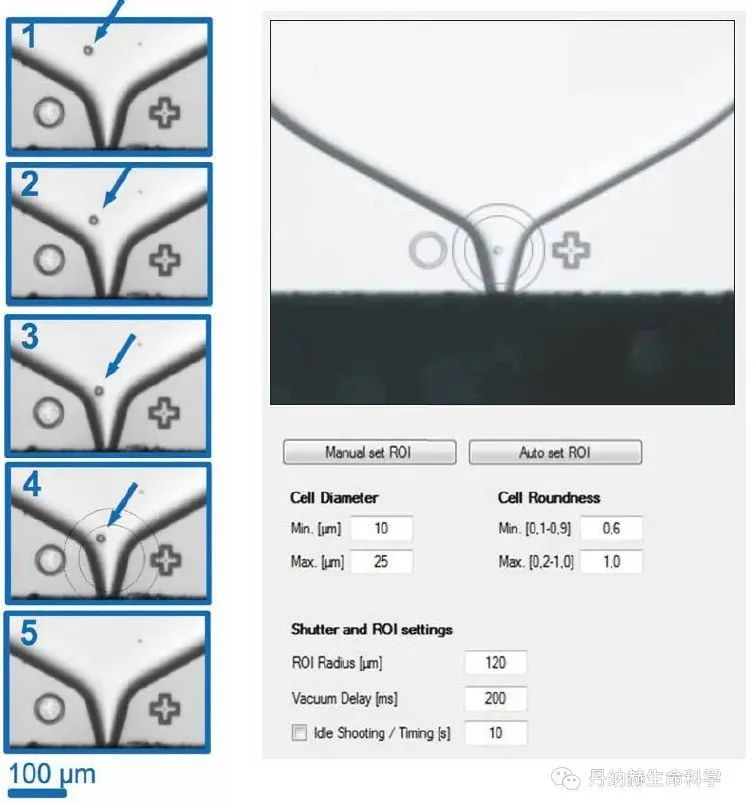
单细胞分选过程图像记录
通过单细胞分离技术获得的单个特异性B细胞,经过单细胞PCR技术从B细胞中扩增IgG重链和轻链可变区基因,并通过测序获得序列信息,再通过基因工程技术,进行载体构建、抗体表达和验证。
单个B细胞抗体技术制备的单克隆抗体,保留了丰富的基因多样性及轻重链可变区天然配对,并且制备效率高,目前已经广泛应用于抗病毒治 疗、神经性疾病治 疗、免疫疾病治 疗等抗体药物的开发。
标签:贝克曼库尔特CytoFLEX SRT流式细胞分选仪 CytEXPERT SRT软件界面 CloneSelect 高通量单细胞分离系统
全部评论(0条)
推荐阅读
-

- 单B细胞抗体技术的关键步骤
- 丹纳赫生命科学旗下贝克曼库尔特的CytoFLEX SRT分选型流式细胞仪是新一代的高效细胞分选平台,适用于多色免疫分型,可进行稳定高表达细胞系的开发、单细胞测序应用等。
-

- 人抗髓鞘少突胶质细胞糖蛋白抗体ELISA试剂盒
- 产品名称:人抗髓鞘少突胶质细胞糖蛋白抗体(IgG)ELISA试剂盒
-

- 人抗髓鞘少突胶质细胞糖蛋白抗体ELISA试剂盒
- 产品名称:人抗髓鞘少突胶质细胞糖蛋白抗体(IgG)ELISA试剂盒
-

- 先导抗体分子产生之路——杂交瘤技术
- 杂交瘤技术又称为单克隆抗体技术:它的主要流程为先进行动物免疫,将特定的抗原注射到哺乳动物体内,使之脾 脏内产生大量分泌针对该抗原的特异性抗体的B淋巴细胞。
-

- 生物物理揭秘抗病毒记忆B细胞遗传记忆 发现记忆免疫对仪器行业发展的重要意义
- 中国科学院国家纳米科学中心孙嘉树团队与北京大学药学院、中国人民解放军总医院第五医学中心、北京大学口腔医院合作,研发出一种基于热泳法的新型基于凝集素糖分子识别的生物传感方法。
①本文由仪器网入驻的作者或注册的会员撰写并发布,观点仅代表作者本人,不代表仪器网立场。若内容侵犯到您的合法权益,请及时告诉,我们立即通知作者,并马上删除。
②凡本网注明"来源:仪器网"的所有作品,版权均属于仪器网,转载时须经本网同意,并请注明仪器网(www.yiqi.com)。
③本网转载并注明来源的作品,目的在于传递更多信息,并不代表本网赞同其观点或证实其内容的真实性,不承担此类作品侵权行为的直接责任及连带责任。其他媒体、网站或个人从本网转载时,必须保留本网注明的作品来源,并自负版权等法律责任。
④若本站内容侵犯到您的合法权益,请及时告诉,我们马上修改或删除。邮箱:hezou_yiqi
















参与评论
登录后参与评论